
Innenraum-Schadstoffe ñ Umweltberatung ñ Information ñ Schadstoff-Forschung
 |
Institut
f■r Angewandte Umweltforschung e.V. Innenraum-Schadstoffe ñ Umweltberatung ñ Information ñ Schadstoff-Forschung |
DEHP (Di(2-ethylhexyl)phthalat) geh—rt zur Gruppe der Phthalsðureester (Phthalate) und ist als Reinsubstanz bei Raumtemperatur eine farblose Fl■ssigkeit. In Tabelle 1 sind einige wesentliche chemische und physikalische Eigenschaften von DEHP aufgef■hrt.
Tabelle 1. Chemische und physikalische Eigenschaften von Di-(2-ethylhexyl)phthalat (NTP-CERHR 2000)
| CAS-Nr. | RN 117-81-7 |
| Summenformel / Molekulargewicht | C24H38O4 / 390,62 |
| Wasserl—slichkeit | 3 çg/L (praktisch unl—slich) |
| Schmelzpunkt / Siedepunkt | -47¯C / 386¯C |
| Dampfdruck | 1,0 x 10-7 mm Hg bei 25¯C |
| Spezifisches Gewicht | 0,986 |
| Chemische Struktur | 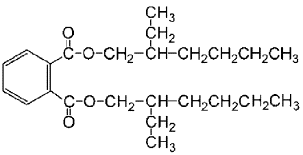 |
DEHP ist der klassische Weichmacher f■r PVC und andere Kunststoffe. Produkte aus diesen Materialien k—nnen 20 bis 80% DEHP enthalten. Bereits seit 1930 wird DEHP als Weichmacher eingesetzt (H—hr und Abel 1989). In Bezug auf seine Einsatzmenge ist DEHP bis heute von allen Phthalaten das wichtigste. In Deutschland wurden 1995 ca. 250.000 Tonnen DEHP produziert, wobei 114.000 Tonnen im Inland verbraucht wurden. Der weltweite jðhrliche Verbrauch liegt bei ■ber 2 Millionen Tonnen (Koch et al. 2003a).
Weil das DEHP nur physikalisch im Kunststoff gebunden ist, entweicht es langsam in die Atmosphðre oder wird bei Kontakt mit Fl■ssigkeiten oder Fetten aus dem Kunststoff herausgel—st. Es ist heute in der Umwelt omniprðsent und bereitet im Labor beim Nachweis geringer Mengen erhebliche Schwierigkeiten.
Neben der Verwendung als Weichmacher wird DEHP in vielen weiteren Bereichen eingesetzt. Als Trðgersubstanz f■r Duftstoffe kommt es in Parfums, Deodorants und K—rperpflegemittel zur Anwendung. Es ist in Nagellacken und Haarsprays enthalten, dient als Formulierungsmittel in Pestizidanwendungen, wird als industrielles L—sungsmittel oder als Schmierstoff eingesetzt und als Additiv in der Textilindustrie verwendet (Koch et al. 2003a). Auch der medizinische Bereich kommt ohne PVC-haltige Produkte wie Blutbeutel, Infusionsbeutel, Dialysebeutel, Katheter, Schlauchsysteme, Kontaktlinsen und viele andere Medizinprodukte nicht aus (Kahl et al. 2003).
Im Innenraum und im tðglichen Leben sind DEHP-haltige Produkte nicht mehr wegzudenken. Einrichtungsgegenstðnde, Dinge des tðglichen Bedarfs oder Baumaterialien k—nnen ganz oder teilweise aus PVC bestehen bzw. DEHP enthalten. Die folgende Liste vermittelt einen Eindruck ■ber die Verbreitung dieses Stoffes.
| Autokindersitz Autohimmel Automobilinnenteile Barbiepuppe Badezimmertextilien Bodenbelðge Couch Computer Dispersionsfarben Duschvorhang Drucker |
Dðmmplatten Dachplanen Elektrokabel Faxgerðt Fernseher Fugenmasse Fahrradtaschen Fahrradgriffe Gummistiefel Gartenschlauch Handy |
Kosmetikverpackung Kunstleder Kopierer Lametta Luftballon Lacke Laptop Lebensmittelverpackg. Matratze Montageschaum Monitor |
Outdoor-Kleidung Puppenkopf Plastikbuch PVC-Bodenbelag Rohre Schuhsohlen Spielzeug Teppichb—den Vinyl-Handschuhe Wandbelðge |
Im Vordergrund einer gesundheitlichen Gefðhrdung durch DEHP stehen nach neuesten Erkenntnissen die Entwicklungs- und Reproduktionstoxizitðt sowie St—rungen des Hormonkreislaufs (endocrine disruption). Die kanzerogene Wirkung, die in fr■heren Tierversuchs-Studien gefunden wurde, wird aufgrund der mangelnden Ébertragbarkeit des tierischen Wirkmechanismus auf den Menschen mehr und mehr relativiert. Erste epidemiologische Daten zur Wirkung von DEHP auf den Menschen sind erst j■ngst erhoben worden. So wird in einer neueren schwedischen Studie (Bornehag et al, 2004) mit erh—hter Konzentration von DEHP im Hausstaub ein Anstieg von Asthma bei Kindern beobachtet. Die meisten Befunde st■tzen sich jedoch nach wie vor auf Tierversuche, die hauptsðchlich mit Ratte oder Maus durchgef■hrt wurden.
Bei inhalativer Aufnahme werden von Erwachsenen etwa 75% der zugef■hrten DEHP-Dosis resorbiert, wðhrend bei Kindern von 100% Bioverf■gbarkeit ausgegangen wird (CSTEE 2002). Nach oraler Aufnahme wurde im Tierversuch eine Resorptionsquote von ca. 50% ermittelt (BfR 2003). Diese Quote wird von den Untersuchungen von Koch et al. (2004) unterst■tzt. Sie fanden, dass 47% einer DEHP-Dosis, die sie einem mðnnlichen Erwachsenen oral applizierten, ■ber den Urin metabolisiert ausgeschieden wurden. Es wird auÔerdem angenommen, dass die Empfindlichkeit gegen■ber DEHP bei oraler Aufnahme h—her ist im Vergleich zu parenteraler Gabe.
Im K—rper wird der Di-Ester DEHP zunðchst schnell zum entsprechenden Mono-Ester Mono-ethylhexylphthalat (MEHP) verstoffwechselt. Danach erfolgt ein weiterer Abbau zu Sekundðrmetaboliten, die ■ber Urin und Stuhl ausgeschieden werden. Im Blut sind DEHP-Metaboliten nur kurzzeitig nachzuweisen und ihre Konzentrationen erreichen bereits nach 4 Stunden wieder Ausgangswerte (Biologische Halbwertszeit ca. 30 min bis 2 h). Deshalb wird die DEHP-Aufnahme ■ber Stoffwechselprodukte im Urin bestimmt. Die Halbwertszeit einer aufgenommenen Dosis betrðgt hier zwischen 12 und 18 Stunden (Koch et al. 2003a). Eine bedeutende Anreicherung im menschlichen K—rper konnte bislang nicht festgestellt werden (NTP-CERHR 2000).
DEHP besitzt keine akute Toxizitðt. Aus einer Fallbeschreibung von zwei erwachsenen Mðnnern geht hervor, dass die orale Aufnahme von 10 g DEHP zu Verdauungsst—rungen f■hrte, wðhrend eine Dosis von 5 g wirkungslos blieb (BfR 2003).
Das empfindlichste Zielorgan der Toxizitðt von DEHP sind bei langfristiger Aufnahme die Hoden (Testes) und die darin befindlichen Sertolizellen, die f■r die Bildung der Spermien verantwortlich sind. Dieser Endpunkt ist gravierend und wird in vielen Studien ausf■hrlich dokumentiert (NTP-CERHR 2000; ATSDR 2002; BfR 2003; CSTEE 2002, 2004). áhnlich empfindlich reagiert das Hormonsystem auf geringe DEHP-Dosen (Akingbemi et al. 2001, 2004; Butte 2004). Die toxikologische Relevanz dieser Verðnderungen wird in Fachkreisen jedoch kontrovers diskutiert (Angerer und Koch 2004). Weitere Wirkungen sind funktionelle Effekte und krankhafte Gewebsverðnderungen an den Nieren sowie Vergr—Ôerungen der Leber, Verðnderungen im Stoffwechsel von Leberzellen sowie Lebertumore. Diese Effekte treten jedoch erst bei 10 bis 100-fach h—heren Dosen auf (BfR 2003).
Entwicklungs und Reproduktionstoxizitðt
DEHP beeintrðchtigt in Tierversuchen die Fortpflanzungsfðhigkeit und die Entwicklung
mðnnlicher Tiere. Zu den festgestellten St—rungen geh—ren verschiedene gewebliche
Verðnderungen in den Hoden und der darin befindlichen Zellen bis hin zum kompletten
Verlust der Spermienbildung. Dabei wurde das DEHP entweder direkt ■ber Trinkwasser und
Nahrung oder ■ber die Muttermilch (exponierte milchgebende Weibchen) zugef■hrt (z.B.
Poon et al. 1997, Arcadi et al. 1998, Wolfe und Layton 2003).
Zur Berechnung einer Dosis, die vom Menschen lebenslang tðglich aufgenommen werden kann, ohne dass eine gesundheitliche Beeintrðchtigung zu erwarten wðre (TDI-Wert - tolerable daily intake) st■tzen sich neuere Berechnungen auf Studien mit entwicklungs- und reproduktionstoxischen Endpunkten. So hat die Europðische Kommission im Rahmen der Altstoffbewertung in der neuesten Risikobewertung von DEHP die Ergebnisse einer Studie von Wolfe und Layton (2003) verwendet, um einen TDI festzulegen (CSTEE 2004). Die Autoren hatten ■ber drei Generationen Sprague-Dawley-Ratten mit DEHP-haltiger Diðt gef■ttert und die testikulðre und Entwicklungstoxizitðt ■berpr■ft. Dabei fanden sie einen NOAEL (No observed adverse effect level, h—chste Dosis ohne unerw■nschte Effekte) von 4,8 mg/kg KG/d. Die Ergebnisse dieser Studie werden robuster eingeschðtzt als die bis 2002 favorisierte Studie von Poon et al. (1997) (CSTEE 2002, 2004).
Hormonelle Aktivitðt
Phthalate k—nnen anti—strogen und antiandrogen wirken. Die Konzentrationen, die im
Tierversuch erste Effekte verursachen, liegen dabei oft unterhalb der Konzentrationen f■r
entwicklungs- bzw. reproduktionstoxische Effekte. So fanden Akingbemi et al. (2001, 2004)
f■r mðnnliche Long-Evans-Ratten im prðpubertðren Alter einen NOAEL von 1 mg/kg KG/d.
Ab 10 mg/kg KG/d stellten sie verðnderte Testosteronspiegel, erh—hte Aktivitðt der
Leydig-Zellen sowie eine erh—hte Estradiol-Produktion fest und schlieÔen aus ihren
Experimenten auf eine indirekte —strogene Wirkung von DEHP. Um eine sichere Abschðtzung
des endokrinen Potenzials des DEHP und der anderen Phthalate treffen sowie die
toxikologische Wirkung auf den Menschen bewerten zu k—nnen, stehen jedoch weitere
Untersuchungen aus (Angerer und Koch 2004).
Kanzerogenitðt und genetische Toxizitðt
Im Tierversuch ist DEHP krebserregend. Die Ébertragbarkeit dieses Befundes auf den
Menschen wird jedoch immer stðrker angezweifelt, da sich die Ergebnisse aus Studien an
Maus und Ratte bei h—heren Tieren wie Affen nicht bestðtigen. AuÔerdem werden immer
mehr Informationen dar■ber gewonnen, in welchem AusmaÔ sich die speziellen
Wirkmechanismen (Peroxisomenproliferation durch PPAR alpha-Induktion) bei Ratte und Mensch
unterscheiden. Die NOAEL von diesem Endpunkt liegen etwa um eine Gr—Ôenordnung h—her
als die entwicklungs- und reproduktionstoxikologischen Endpunkte (ATSDR 2002; CSTEE 2002).
Gentoxischen Effekte von DEHP konnten meistens nicht festgestellt werden. Das belegen Untersuchungen einer groÔe Anzahl verschiedener Testsysteme (CSTEE 2002).
Erste epidemiologische Studien der Wirkung von Phthalaten auf den Menschen wurden von Duty et al. (2003a,b) durchgef■hrt. Dabei wurden Urin- und Spermienproben von 168 Mðnnern aus Paaren mit verminderter Fruchtbarkeit untersucht. Im Urin wurden acht Phthalate analysiert, darunter der primðre DEHP-Metabolit MEHP. Bei den Spermien wurde ihre Konzentration, Beweglichkeit und DNA-Integritðt ermittelt. F■r MEHP und drei weitere Phthalate konnten keine signifikanten Korrelationen zwischen Phthalat-Konzentrationen und Spermien-Parametern gefunden werden, wðhrend f■r andere Phthalate manche Korrelationen signifikant waren. Die Autoren werten diesen Befund als Indiz f■r eine unterschiedliche Spermientoxizitðt verschiedener Phthalate.
Die toxikologische Datenlage hat zu einer Reihe von kritischen Einschðtzungen und Verboten gef■hrt. Die MAK-Werte-Kommission hat DEHP in Kategorie 4 der Krebserzeugenden Arbeitsstoffe eingestuft (Stoffe mit krebserzeugender Wirkung, bei denen genotoxische Effekte keine oder nur eine untergeordnete Rolle spielen; DFG 2003). Wðhrend die US-Umweltagentur EPA DEHP als beim Menschen wahrscheinlich Krebs erregend (Gruppe B2) einstuft, klassifiziert die Internationale Agentur f■r Krebsforschung (International Agency for Research on Cancer, IARC) den Stoff in ihre Kategorie 3 (Kanzerogenitðt konnte nur unzureichend nachgewiesen werden). Das Nationale Toxikologie Programm der USA (NTP) bewertet zusammen mit dem Zentrum f■r die Abschðtzung der Risiken f■r die menschliche Reproduktion (CERHR - das Zentrum setzt sich aus allen relevanten Umweltbeh—rden der USA zusammen) DEHP als "ernsthaft bedenklich f■r die menschliche Fortpflanzung oder Entwicklung" (NTP-CERHR 2000). Im Sinne der Europðischen Wasserrahmenrichtlinie ist DEHP ein "prioritðrer Schadstoff" und wird von der EU als "fortpflanzungsgefðhrdend" eingestuft (WWF 2004).
Seit 1999 hat die Kommission der Europðischen Gemeinschaft sechs Weichmacher in Spielzeug- und Babyartikeln f■r Kinder unter 3 Jahren befristet verboten (EU 1999). Bisher wurde das Verbot fristgerecht alle 3 Monate verlðngert. In Kosmetika sind DEHP und Dibutylphthalat seit 2003 EU-weit verboten (EU 2003a). Ab Dezember 2004 wird die Verwendung dieser Stoffe in allen Konsumentenprodukten in der EU eingeschrðnkt (EU 2003b). In østerreich sind Phthalate - mit Ausnahmen - in Lebensmittelverpackungen verboten (BGBl 2003). Die Kunststoffkommission des deutschen Bundesinstituts f■r Risikobewertung empfiehlt, dass DEHP enthaltende Folien aus Weich-PVC, die in Kontakt mit Lebensmitteln kommen k—nnen, nicht mehr verwendet werden (BfR 2003).
Durch den massiven industriellen Einsatz von DEHP ist dieser Stoff in der Umwelt ubiquitðr (■berall vorhanden) und lðsst sich damit in allen Medien nachweisen, denen der Mensch ausgesetzt ist.
Lebensmittel
Petersen und Breindahl (2000) analysierten Weichmacher-Gehalte (darunter DEHP) von
Lebensmitteln in Dðnemark, die von einem Proband innerhalb von 24 h verzehrt wurden (n =
29). Die Lebensmittel wurden im Rahmen einer gr—Ôeren Ernðhrungsstudie
zusammengestellt. Normalisiert auf eine tðgliche Kost von 10 MJ Energie, fanden sie
durchschnittliche DEHP-Gehalte zwischen 190 und 300 çg/kg (Maximum: 1100 çg/kg). Dieses
Ergebnis deckt sich mit einer Schweizer Studie (BfR 2003). In einer Untersuchung aus
England wurden keine Gehalte ■ber 20 çg/kg KG/d (Mikrogramm pro Kilogramm K—rpergewicht
pro Tag) gefunden. F■r Deutschland gibt es keine reprðsentativen Daten (BfR 2003).
Babynahrung und Muttermilch
Das CSTEE (2004) zitiert eine Studie, in der 39 Proben Babynahrung von 14 verschiedenen
Marken untersucht wurden. Basierend auf der gr—Ôten gefundenen Konzentration von 440
çg/kg, wurde eine Tagesdosis f■r ein 3 - 12 Monate altes Baby von 8 çg/kg KG/d
abgeschðtzt. Petersen und Breindahl (2000) kamen bei ihrer Untersuchung von Babynahrung
und Instant-Produkten f■r Kinder (jeweils n = 11) auf ðhnliche Ergebnisse. Ihre
ermittelte maximal mittlere Dosis betrug 7 çg/kg KG/d (Maximum: 16 çg/kg KG/d).
In Untersuchungen der Muttermilch wurde ein maximaler Gehalt von 160 çg/kg ermittelt (CSTEE 2004). Die daraus resultierenden Tagesdosen wurden zu 21 çg/kg KG/d (0 bis 3 Monate altes Baby) bzw. 8 çg/kg KG/d (3 bis 12 Monate altes Baby) errechnet.
Trinkwasser
Im Trinkwasser werden ■blicherweise Gehalte bis 1 çg/L DEHP gefunden, in
Trinkwasserbrunnen auch schon Werte bis 170 çg/L (BAUCH 1991). In Holland wurden bis zu
3,5 çg/L DEHP im Trinkwasser ermittelt (ENDS 1999).
Luft und Schwebstaub
In der Risikoabschðtzung der Europðischen Union f■r DEHP wird von einem
Worst-Case-Szenario ausgegangen (CSTEE 2004). Bei 100% Luftsðttigung (5,3 çg/m°) plus
das 3-fache durch DEHP-haltigen Feinstaub wird eine Konzentration von 21,2 çg/m°
abgeschðtzt. Untersuchungen zeigen jedoch, dass tatsðchlich gemessene Konzentrationen um
den Faktor 10 bis 100 darunter liegen. Sheldon et al. (1993) fanden in 125 kalifornischen
Wohnungen im Mittel 0,110 çg/m° DEHP, das 90. Perzentil betrug 0,240 çg/m°. (12 h
Messung, Aerosole und Gasphase erfasst). Die Untersuchung der AuÔenluft erbrachte im
Mittel 0,028 çg/m° (90. Perzentil 0,065 çg/m°). Fromme et al. (2004) untersuchten
Berliner Wohnungen und Kindergðrten. In den Wohnungen (n = 59) fanden sie f■r DEHP ein
95.-Perzentil von 0,39 çg/m°, in den Kindergðrten wurden 1,51 çg/m° gemessen
(95.-Perzentil).
Hausstaub
F■r Hausstaub liegt ein umfangreiches Datenkollektiv vor. Trotz stark unterschiedlicher
Methoden in der Probenahme und der Analyse liegen alle Ergebnisse in einer vergleichbaren
Gr—Ôenordnung. In Tabelle 2 sind ausgewðhlte Studien von deutschen Haushalten
aufgef■hrt.
| Tabelle 2. DEHP-Gehalte im Hausstaub (mg/kg). |
| Studie | n | Fraktion | Median | 90.-Perz | 95.-Perz | Bereich |
| ARGUK (2004) | 499 | 2 mm | 486 | 2190 | 3660 | 5 - 32055 |
| Fromme et al. (2004) | 30 | Feinstaub | 703 | 1542 | 231 - 1763 | |
| Becker et al. (2004) | 2 mm | 416 | 978 | 1190 | 0,2 - 7530 | |
| Butte et al. (2001) | 286 | 63 çm | 740 | 2600 | max 12000 | |
| HH (2002) | 65 | 63 çm | 600 | 1600 | ||
| P—hner et al. (1997) | 272 | Gesamt | 450 | 1600 | 2000 | 0,7 - 8600 |
Boden
Persson et al. (1978, zitiert in IPCS 1992) fanden in Bodenproben aus Finnland einen
Maximalgehalt von 500 çg/kg. Die Proben wurden in der Nðhe eines DEHP-produzierenden
Betriebes entnommen.
Kinderspielzeug
Spielzeug und Babyartikel f■r Kinder unter 3 Jahren d■rfen in der EU seit 1999 nicht
mehr als 0,1% Gewichtsanteil Phthalate enthalten, darunter DEHP (EU 1999). Das
Inverkehrbringen von Spielzeug mit h—heren Gehalten ist verboten. Produkte ðlteren
Datums k—nnen jedoch DEHP und andere Weichmacher abgeben. Das CSTEE (1998) schðtzt, dass
bei durchschnittlicher Benutzung dieser Produkte Kleinkinder mit einem K—rpergewicht von
8 kg eine Dosis von 200 çg/kg KG/d aufnehmen k—nnen.
Kleidung
Durch Bekleidung aus PVC k—nnen Weichmacher von der Haut aufgenommen werden. Es ist
jedoch sehr schwierig, diesen Expositionspfad zu quantifizieren, und jeder Versuch bleibt
spekulativ. Um dennoch einen Begriff f■r die Gr—Ôenordnung einer m—glichen Exposition
zu erhalten, hat die amerikanische Kommission f■r Produktsicherheit (U.S. Consumer
Product Safety Commission, CPSC) die Mengen abgeschðtzt, welche an dem Weichmacher DINP
unter bestimmten Bedingungen durch das Tragen von Regenmðnteln bzw. Sandalen aus PVC von
Kindern und Erwachsenen aufgenommen werden k—nnen (CPSC 2001). In Ermangelung an
entsprechenden Daten f■r DEHP wird analog zu CSTEE (1998) angenommen, dass die Ergebnisse
f■r DINP auch f■r DEHP gelten (Tabelle 3).
| Tabelle 3. Dermale DEHP-Exposition durch Tragen Weichmacherhaltiger Bekleidung. Rahmenbedingungen Regenmantel Kleinkind: 400 cmý exponierte Flðche, 4 h pro Tag an 30 Tagen im Jahr. |
| Alter | K—rpergewicht | Produkt | Exposition (çg/kg KG/d)* |
|
| Erwachsener | 70 kg | Regenmantel | 0,45* - 11* | |
| Kleinkind | 1,5 - 3 Jahre | 10 kg | Regenmantel | 3,2 - 79 |
| Erwachsener | 70 kg | Sandalen | 3,9 - 98 | |
| Kleinkind | 1,5 - 3 Jahre | 10 kg | Sandalen | 14 - 340 |
| *je nach verwendetem Expositionsmodell (CPSC 2001) |
Vinyl-Handschuhe
Auch durch das Tragen von Vinyl-Handschuhen kann DEHP aufgenommen werden. Das BfR
schðtzt, dass bei tðglichem mehrst■ndigen Tragen solcher Handschuhe zwischen 3 und 119
çg/kg KG/d je nach verwendetem Rechenmodell aufgenommen werden k—nnen (BfR 2003). Das
CSTEE (2002) f■hrt als Ergebnis einer Studie eine Aufnahmemenge von 6,7 çg/kg KG/d an.
Eine groÔe Anzahl von Medizinprodukten wie Schlauchmaterial oder Blut- und Infusionsbeutel k—nnen DEHP enthalten. Durch den vielfðltigen Einsatz im Krankenhaus kann auf diesem Wege DEHP ■ber alle Pfade (inhalativ, oral, dermal und intraven—s) in besonderem MaÔe aufgenommen werden. Neben Hðmolyse-Patienten ist die Situation f■r Fr■h- und Neugeborene ðuÔerst Besorgnis erregend. Bei ihnen f■hren Schlauchmaterialien f■r Ernðhrung, Beatmung, extrakorporale Membranoxygenation (ECMO) und Infusionen zu stark erh—hten Expositionen. Kahl et al. (2003) zitieren tðgliche Belastungen von mindestens 5000 çg/kg KG/d (Daten von Loff et al. 2000 bei 2 kg KG und 100% Resorption) bzw. an anderer Stelle 1800 çg/kg KG/d. Diese Werte reichen an Konzentrationen, die im Tierversuch bereits Schðdigungen zeigten, heran oder ■berschreiten diese (Poon et al. 1997; Wolfe und Layton 2003). Da Krankenhausaufenthalte jedoch eine auÔergew—hnliche Lebenssituation darstellen, wird dieses Thema hier nicht weiter behandelt.
Zur Abschðtzung der gesamten ðuÔeren Exposition gegen■ber DEHP f■r Erwachsene und Kinder wurden f■r beide Personengruppen Rahmenparameter festgelegt, die in Tabelle 4 zusammengefasst sind. Die Standard-Annahmen f■r ein Kleinkind beziehen sich auf ein Alter von ca. 12 Monate. In diesem Alter ist von einer maximalen Staubaufnahme durch "Hand-in-den-Mund"-Verhalten (engl. Mouthing oder Picking) auszugehen, wðhrend die Ernðhrung meist noch auf besonderer Babynahrung basiert. Wðhrend Nahrung, Trinkwasser und Luft selbstverstðndlich tðglich aufgenommen werden, ist dies bei Hausstaub und Boden nicht der Fall. Hier wurde eine auf das Jahr verteilte Exposition abgeschðtzt. Die folgende Berechnung (Tabellen 4 bis 10) setzt konservative Rahmenbedingungen. Die tatsðchliche Belastung kann je nach Grundannahmen auch um ein Vielfaches h—her liegen.
| Tabelle 4. Standard-Annahmen f■r die Abschðtzung der ðuÔeren Exposition gegen■ber DEHP f■r Erwachsene und Kleinkinder |
| Erwachsener | Kleinkind | |
| K—rpergewicht (KG) | 75 kg | 10 kg |
| Inhalativer Aufnahmepfad | ||
| Atemrate | 20 m°/d | 6 m°/d |
| Resorptionsquote1) | 75% | 100% |
| Oraler Aufnahmepfad | ||
| Resorptionsquote2) | 50% | 50% |
| Aufnahmerate Staub | 20 mg/d | 100 mg/d |
| Expositionshðufigkeit Staub | 100 d/a | 300 d/a |
| Aufnahmerate Boden | 20 mg/d | 100 mg/d |
| Expositionshðufigkeit Boden | 50 d/a | 100 d/a |
| Trinkwasser-Tagesverzehr | 2 L/d | 1 L/d |
| 1) CSTEE 2002; Gundert-Remy 2004 |
| 2) Koch et al. 2003a; BfR 2003 |
| Tabelle 5. Tðgliche DEHP-Aufnahme ■ber die Nahrung. |
| DEHP-Zufuhr (çg/d) |
DEHP-Zufuhr pro kg KG (çg/kg KG/d) |
DEHP-Aufnahme pro kg KG (çg/kg KG/d) |
DEHP-Aufnahme (çg/d) |
|
| Erwachsener | 300* | 4,0 | 2,0 | 150 |
| Kleinkind | - | - | 7,0** | - |
| * Maximaler Mittelwert f■r einen Erwachsenen (Petersen und Breindahl 2000) |
| ** Maximaler Mittelwert von Fertignahrung f■r ein Kleinkind (Petersen und Breindahl 2000) |
| Tabelle 6. Tðgliche DEHP-Aufnahme ■ber das Trinkwasser |
| DEHP-Gehalt (çg/L)* |
DEHP-Zufuhr (çg/d) |
DEHP-Zufuhr pro kg KG (çg/kg KG/d) |
DEHP-Aufnahme pro kg KG (çg/kg KG/d) |
DEHP-Aufnahme (çg/d) |
|
| Erwachsener | 3,5 | 7,0 | 0,093 | 0,047 | 3,5 |
| Kleinkind | 3,5 | 3,5 | 0,35 | 0,18 | 1,8 |
| * Maximalwert, der in Trinkwasser in Holland gefunden wurde (ENDS 1999) |
| Tabelle 7. Tðgliche DEHP-Aufnahme ■ber die Luft |
| DEHP-Gehalt (çg/g)* |
DEHP-Zufuhr (çg/d) |
DEHP-Zufuhr pro kg KG (çg/kg KG/d) |
DEHP-Aufnahme pro kg KG (çg/kg KG/d) |
DEHP-Aufnahme (çg/d) |
|
| Erwachsener | 0,39* | 7,8 | 0,10 | 0,078 | 5,9 |
| Kleinkind | 0,39* | 2,3 | 0,23 | 0,47** | 2,3 |
| * 95.-Perzentil der Studie von Fromme et al. (2004). Es wurden 59 Berliner Wohnungen untersucht. |
| ** Die berechnete DEHP-Aufnahme wurde zusðtzlich mit 2 multipliziert, um das h—here Atemminutenvolumen von Kindern zu ber■cksichtigen (Straff 2004). |
| Tabelle 8. Tðgliche DEHP-Aufnahme ■ber den Hausstaub |
| DEHP-Gehalt (çg/g)* |
DEHP-Zufuhr (çg/d) |
DEHP-Zufuhr pro kg KG (çg/kg KG/d) |
DEHP-Aufnahme pro kg KG (çg/kg KG/d) |
DEHP-Aufnahme (çg/d) |
|
| Erwachsener | 978* | 5,4 | 0,072 | 0,036 | 2,7 |
| Kleinkind | 978* | 81 | 8,1 | 4,0 | 40 |
| * 90.Perzentil im Umwelt-Survey 1998 (Becker et al. 2002) |
| Tabelle 9. Tðgliche DEHP-Aufnahme ■ber den Boden |
| DEHP-Gehalt (çg/g)* |
DEHP-Zufuhr (çg/d) |
DEHP-Zufuhr pro kg KG (çg/kg KG/d) |
DEHP-Aufnahme pro kg KG (çg/kg KG/d) |
DEHP-Aufnahme (çg/d) |
|
| Erwachsener | 500* | 1,4 | 0,018 | 0,0092 | 0,69 |
| Kleinkind | 500* | 14 | 1,4 | 0,69 | 6,9 |
| * Persson et al. (1978, zitiert in IPCS 1992) |
In Tabelle 10 wird die DEHP-Gesamtexposition abgeschðtzt, indem die DEHP-Aufnahmen f■r Lebensmittel, Trinkwasser, Luft, Hausstaub und Boden summiert werden. Die Aufnahme von DEHP ■ber diese Medien stellt eine Grundbelastung dar, die sich nicht oder nur beschrðnkt durch individuelles Verhalten beeinflussen lðsst. Die dermale Exposition durch Produkte des tðglichen Bedarfs (z.B. Kinderspielzeug, Bekleidung, Vinylhandschuhe) wurde in die Abschðtzung der Grundlast nicht mit einbezogen, da die Exposition individuell stark variieren kann, je nach Art und Beschaffenheit der Bekleidung, den Tragegewohnheiten und einer Vielzahl weiterer Faktoren, die den Ébergang vom Material auf die Haut bestimmen. Da die individuelle DEHP-Aufnahme um ein Vielfaches steigen kann, wenn solche Produkte benutzt werden (vgl. Abschnitt 5.3.), ist es wenig sinnvoll, sie auf einen Durchschnitt herunter zu rechnen und der Grundlast hinzuzuf■gen.
| Tabelle 10. DEHP-Grundlast f■r Erwachsene und Kleinkinder. Summe der tðglichen DEHP-Aufnahme ■ber die Expositionspfade Nahrung, Trinkwasser, Luft, Hausstaub und Boden |
| DEHP-Zufuhr (çg/d) |
DEHP-Zufuhr pro kg KG (çg/kg KG/d) |
DEHP-Aufnahme pro kg KG (çg/kg KG/d) |
DEHP-Aufnahme (çg/d) |
|
| Erwachsener | 322 | 4,3 | 2,2 | 163 |
| Kleinkind | - | - | 12 | - |
Die Abschðtzung deckt sich gut mit den Angaben anderer Autoren. Doull et al. (1999) rechen mit einer durchschnittlichen Belastung der Allgemeinbev—lkerung aus Umweltbelastungen von 3 bis 30 çg/kg KG/d. MAFF (1996) geben als 97,5. Perzentil 27 çg/kg KG/d an, wðhrend Meek und Chan (1994) f■r die Altersgruppe der 20- bis 70-jðhrigen 5,8 çg/kg KG/d annehmen.
Aus unserer Abschðtzung wird deutlich, dass Kleinkinder in einem viel gr—Ôeren MaÔe durch DEHP belastet werden als Erwachsene. Die von ihnen tðglich resorbierte DEHP-Dosis von 12 çg/kg KG/d liegt um das 6-fache ■ber der von Erwachsenen. Auch dieses Ergebnis wird von anderen Autoren bestðtigt. Meek und Chan (1994) schðtzen bei 0,5- bis 4-jðhrigen die tðgliche Aufnahme auf 19 çg/kg KG/d. Diese Altersgruppe ist ihren Berechnungen nach am h—chsten belastet und betrðgt das 3,3-fache der Belastung von Erwachsenen. Gleichzeitig ist sie die empfindlichste Subpopulation.
Koch et al. (2003b) haben den Urin von 85 Individuen aus dem s■ddeutschen Raum (Alter 7 - 64) auf sekundðre Stoffwechselprodukte (Metaboliten) von DEHP untersucht, um daraus deren gesamte DEHP-Aufnahme zu berechnen. Die Untersuchung von DEHP-Sekundðrmetaboliten (5OH-MEHP und 5oxo-MEHP) ist neu und mit wesentlich geringeren Fehlern behaftet als ðltere Methoden, die auf der Bestimmung von primðren Metaboliten (MEHP bzw. 2-Ethylhexanol) basieren. Insbesondere vermeidet die neue Methode Verfðlschungen, die durch mit DEHP verunreinigtem Laborgerðt hervorgerufen werden. Die Autoren fanden wesentlich h—here Belastungen als bisher angenommen. Wðhrend Studien, die auf der MEHP-Analytik basieren, ein 95. Perzentil von um die 3 çg/kg KG/d angeben (z.B. Kohn et al. 2000, David et al. 2000), fanden Koch et al. (2003b) Werte, die um mindestens eine Zehnerpotenz h—her liegen (Tabelle 11).
M—glicherweise neigt diese Untersuchung jedoch zu einer Éberschðtzung der inneren Belastung, da von den gemessenen Sekundðrmetaboliten auf die DEHP-Belastung mit Faktoren hochgerechnet wurde, die von Schmidt und Schlatter (1985) ermittelt wurden. In einer neuen Untersuchung zur Metabolisierung von DEHP fanden Koch et al. (2004), dass im Urin wesentlich mehr DEHP-Metaboliten ausgeschieden werden (47%), als Schmidt und Schlatter fanden (10-25%).
| Tabelle 11. Tðgliche Aufnahme der Allgemeinbev—lkerung (Erwachsene) an DEHP, berechnet aus unterschiedlichen Bestimmungsmethoden (çg/kg KG/d). |
| Autor | Median | 95. Perz. | Bereich | Methode |
| Koch et al. (2003b) | 13,8 | 52,1 | 2,6 - 166 | Sekundðrmetaboliten |
| Kohn et al. (2000) | 0,71 | 3,6 | < BG - 46 | MEHP |
| David et al. (2000) | 0,6 | 3,05 | < BG - 38,5 | MEHP |
Dass Kinder h—her belastet sind als Erwachsene konnte von Koch et al. (2003c) ebenfalls bestðtigt werden. Nach einer Untersuchung von Kindergartenkindern und deren Eltern wurde festgestellt, dass die Kinder signifikant h—here Gehalte an DEHP-Sekundðrmetaboliten im Urin aufwiesen. Im Vergleich lagen die Mittelwerte, Mediane und 95.-Perzentile bei den Kindern um den Faktor 1,5 bis 1,9 h—her.
Der Befund von Koch et al. (2003b) weist darauf hin, dass die ðuÔere Belastung m—glicherweise h—her ist als bislang angenommen und damit L■cken in der Abschðtzung der ðuÔeren Belastung existieren.
Auf der Basis von Studien an Tieren haben verschiedene Institutionen Aufnahmemengen an DEHP berechnet, die sie beim Menschen f■r noch tolerabel halten. Die Ergebnisse unterscheiden sich um mehr als eine Zehnerpotenz (Tabelle 12).
Der niedrigste TDI wird vom niederlðndischen Nationalen Institut f■r Volksgesundheit und Umwelt (RIVM) angegeben. Er basiert auf der Studie von Poon et al. (1997), die einen NOAEL von 3,7 mg/kg KG/d im Versuch mit Ratten ermittelt hatten (vgl. Abschnitt 4.3.1. Entwicklungs- und Reproduktionstoxizitðt). Als Endpunkt wurde in dieser Studie die Schðdigung (Vakuolisierung) von Sertolizellen in den Hoden untersucht. Da dieses Ergebnis vom RIVM als relevant sowohl f■r mðnnliche Jungtiere als auch erwachsene Tiere eingestuft wird, wurde bei der Berechung des TDI ein Unsicherheitsfaktor von 10 angewendet, um auf eine lebenslange Exposition zu extrapolieren. Ein Unsicherheitsfaktor von 100 wurde verwendet, um die inter- und intraspezifische Variation zu ber■cksichtigen. Mit diesen Faktoren gelangte man zu einem TDI von 4 çg/kg KG/d. Dieser TDI wird vom RIVM als "hoch verlðsslich" eingestuft. Das bedeutet, dass die Autoren die toxikologische Datenbasis zu DEHP als relativ vollstðndig einstufen, dass ausreichende Daten insbesondere zur chronischen Toxizitðt vorliegen, und dass international ein ausreichender Konsens besteht in Bezug auf die toxischen Effekte (Baars et al. 2001). Am TDI des niederlðndischen RIVM wird deshalb im nðchsten Abschnitt die in Abschnitt 6. abgeschðtzte Exposition von Kleinkindern gemessen.
Wir halten dieses Vorgehen auch dadurch f■r legitimiert, dass DEHP bis auf weiteres der einzige phthalatische Weichmacher ist, dessen Aufnahme durch den Mensch genauerer Beobachtung unterliegt. In der Risikoabschðtzung steht er deshalb einstweilen nicht nur f■r sich alleine, sondern hat auch Stellvertreterfunktion f■r eine Vielzahl weiterer industriell genutzter Phthalate. Koch et al. (2003b) haben gezeigt, dass zusammen mit DEHP oft weitere Phthalate in hohen Konzentrationen im Urin nachgewiesen werden k—nnen. Dabei gehen Koch et al. (2003a) von einer gleichgerichteten, additiven toxischen Wirkung dieser Verbindungen aus. Ein m—glicherweise ■berschðtzter Sicherheitsabstand bei DEHP k—nnte also eine m—glicherweise unterschðtzte Phthalat-Gesamtaufnahme kompensieren.
| Tabelle 12. Richtwerte verschiedener Institutionen zur tolerierbaren DEHP-Aufnahmemenge |
| Land / Institution | Richtwert (çg/kg KG/d) |
Bezeichnung | Endpunkt | Autor |
| Niederlande: Rijksinstituut voor Volksgezondheid en Milieu (RIVM) | 4 | TDI (MPR) | Reproduktionstoxizitðt (Schðdigung Sertolizellen) | Baars et al. 2001 |
| USA: Environmental Protection Agency (EPA) | 20 | RfD | Erh—htes Lebergewicht | IRIS 2004 |
| World Health Organization (WHO) | 25 | TDI | Peroxisomen-Proliferation in der Leber | WHO 1996, zitiert nach Baars et al. 2001 |
| EU: Scientific Committee on toxicity, ecotoxicity and the environment (CSTEE) | 48 | TDI | Entwicklungstoxizitðt und testikulðre Toxizitðt | CSTEE 2004 |
| Deutschland: Umweltbundesamt | 50 | TRD | Lebertoxizitðt | Hassauer et al. 1993, zitiert nach Baars et al. 2001 |
| USA: Agency for Toxic Substances and Disease Registry | 60 | MRL | Testikulðre Toxizitðt | ATSDR 2002 |
| TDI: Tolerable Daily Intake; MPR: Maximum Permissible Risk Level; RfD:
Reference Dose (f■r chronische orale Exposition); TRD: Tolerierbare resorbierte Dosis; MRL: Minimal Risk Level (f■r chronische orale Exposition) |
Eine Exposition von Kleinkindern gegen■ber DEHP in der H—he von 12 çg/kg KG/d ist nicht ungew—hnlich, wie die Expositionsabschðtzung in Abschnitt 6. zeigt. Mit einer solchen Grundbelastung wird der TDI des RIVM um das 2-fache ■berschritten. In Tabelle 13 ist die Verteilung der einzelnen Pfade auf die Grundbelastung dargestellt.
Nicht mit eingegangen in diese Abschðtzung ist die Belastung durch das Lutschen oder Kauen von DEHP-haltigem Kinderspielzeug oder das Tragen von Kleidung aus PVC wie Regenmðntel, Gummistiefel oder Sandalen. Das ■ber diesen Weg freigesetzte und aufgenommene DEHP ■bersteigt selbst bei normaler Benutzung die Grundbelastung um ein Vielfaches: Durch das Lutschen oder Kauen von Kinderspielzeug k—nnen bis zu 200 çg/kg KG/d aufgenommen werden (CSTEE 1998). Éber die Haut k—nnen tðglich bis zu 79 (Regenmantel) bzw. 340 (Sandalen) çg/kg KG/d aufgenommen werden (CPSC 2001).
| Tabelle 13. Zusammensetzung der gesamten tðglichen DEHP-Aufnahme (Grundbelastung) aus den einzelnen Expositionspfaden beim Kleinkind (çg/kg KG/d). |
| Nahrung | Trinkwasser | Luft | Staub | Boden | Gesamt | |
| Tagesdosis | 7 | 0,175 | 0,144 | 4 | 0,7 | 12 |
| Anteil | 58,3% | 1,4% | 1,2% | 33,3% | 5,8% | 100% |
Nach ihrer Bedeutung gewichtet ergibt sich daher f■r die Expositionspfade folgendes Bild:
Kleidung und Kinderspielzeug > Nahrung > Hausstaub > Boden > Trinkwasser > Luft
Die Belastung durch DEHP-haltiges Kinderspielzeug stellt eine der wichtigsten und intensivsten Belastungsquellen dar. Deshalb wurde 1999 DEHP-haltiges Spielzeug und Babyartikel f■r Kinder unter 3 Jahren EU-weit verboten (EU 1999). Altes Spielzeug, das aus PVC besteht, oder dessen Materialart nicht bekannt ist, sollte deshalb nicht "weitervererbt" und weiterverwendet werden! Beim Neukauf auÔerhalb Europas sollte auf Kennzeichnungen wie "PP" (Polypropylen) oder "PE" (Polyethylen) geachtet werden. Diese Materialien sind weniger bedenklich.
Die Belastung durch DEHP-haltige Kleidung besitzt einen ðhnlich hohen Stellenwert wie das Kinderspielzeug. Trotzdem ist dieser Bereich noch nicht reguliert. Man sollte deshalb PVC-haltige Produkte, die bei Kindern in direktem Kontakt mit der Haut stehen k—nnen, auf jeden Fall vermeiden und nach Alternativen suchen! Diese bestehen zum Beispiel im Kauf von Gummistiefeln aus echtem Gummi oder Jacken aus gewachster Baumwolle. Auch Polyester und Polyamid sind als Bekleidungsmaterial weniger schðdlich.
Der Nahrungspfad stellt im Rahmen der Grundbelastung die wichtigste Belastungsquelle dar und f■hrt f■r sich alleine zu einer Éberschreitung des TDI um 75%. Eine Regulation dieses Pfades wird aber zunehmend in Angriff genommen, wie eine Reihe neuer Verordnungen belegen. Darunter fallen z.B. die EU-weite Beschrðnkung der Verwendung von Weichmachern in Konsumentenprodukten ab Dez 2004 oder das Verbot von vielen Phthalaten in Lebensmittelverpackungen in østerreich (EU 2003b).
Die M—glichkeit der pers—nlichen Einflussnahme auf die DEHP-Aufnahme durch die Nahrung ist stark beschrðnkt. Bei dem Versuch, Lebensmittel zu meiden, die in Kunststoff verpackt sind, kann die Palette der akzeptablen Nahrungsmittel stark eingeschrðnkt sein. Prinzipiell empfiehlt es sich dort einzukaufen, wo die Transportketten kurz sind (z.B. beim Direkterzeuger) und die Lebensmittel nicht aufwðndig verpackt und lange aufbewahrt werden m■ssen, oder der bevorzugte Einkauf von losem Gut.
Der Hausstaubpfad alleine sch—pft ebenfalls den TDI vollstðndig aus. Insgesamt stellt er die zweitwichtigste Belastungsm—glichkeit dar, kann aber bei Kindern mit stðrkerem Hand-zu-Mund-Verhalten schnell zur wichtigsten Belastungsquelle aufsteigen und den TDI-Wert um ein vielfaches ■berschreiten. Calabrese et al. (1989) fanden, dass solche Kinder mehr als 1 g Hausstaub pro Tag verschlucken k—nnen.
Die M—glichkeit der pers—nlichen Einflussnahme auf die DEHP-Aufnahme durch den Hausstaub ist relativ groÔ. Die wichtigste MaÔnahme besteht in der Vermeidung von PVC-B—den und anderen PVC-haltigen Produkten und Baumaterialien. Dar■ber hinaus kann hðufiges Wischen und Beseitigen des Staubes die Exposition gegen■ber DEHP maÔgeblich reduzieren.
Die anderen Pfade (Trinkwasser, Luft, Boden) beanspruchen zusammen nur 8,4% der Gesamtbelastung und sind deshalb wenig bedeutend.
Somit stellt der Hausstaub den zweitwichtigsten Aufnahmepfad f■r Kleinkinder dar mit Tendenz hin zum wichtigsten. Eine Regulierung dieses Pfads hat bisher jedoch noch nicht stattgefunden. Im Abschnitt 10. schlagen wir deshalb die Etablierung eines toxikologisch begr■ndeten Richtwerts f■r die DEHP-Belastung des Hausstaubes vor.
Wir haben mit dem TDI des RIVM einen niedrigen TDI gewðhlt (Tabelle 12). Andere Organisationen berechnen TDIs, die um etwa eine Gr—Ôenordnung h—her liegen k—nnen. Wðre das vorgestellte Szenario der ðuÔeren Exposition weniger kritisch einzustufen, wenn man einen h—heren TDI zur Beurteilung wðhlen w■rde? Das hier vorgestellte Expositionsszenario geht von eher konservativen Annahmen aus. Bei der Wahl von Rahmenbedingungen, die in stðrkerem MaÔe Extremfðlle ber■cksichtigen (z.B. Wahl von Maximalkonzentrationen in Lebensmitteln oder im Hausstaub), oder von ung■nstigeren Voraussetzungen ausgehen (z.B. Einbezug der dermalen Exposition in die Grundlast, eine 100%ige orale Resorption bei Kindern oder eine h—here Staubaufnahme), gelðnge man leicht zu 10-fach h—heren Expositionen und damit in einen Bereich, in dem auch h—here TDIs ausgesch—pft werden.
Ein Richtwert zur Begrenzung der DEHP-Belastung von Hausstðuben ist erforderlich, um die Bedeutung dieses Expositionspfades f■r Kleinkinder ins —ffentliche Bewusstsein zu r■cken. Er k—nnte zum Motor f■r eine verstðrkte Éberwachung dieser gefðhrlichen Belastung und so zu PrðventionsmaÔnahmen, anspruchsvolle und effiziente Entstaubung und Quellenvermeidung f■hren. Ein solcher Richtwert wðre ein Beitrag zur Gefahrenabwehr sowie f■r die Gesundheitsf—rderung.
Wir schlagen deshalb einen Richtwert f■r DEHP-Belastungen des Hausstaubes f■r Kleinkinder vor von
100 çg DEHP/g Hausstaub
Dieser Vorschlag orientiert sich an der MaÔgabe, dass von einem Expositionspfad m—glichst nicht mehr als 10% der Tolerierbaren Resorbierten Dosis (TRD) beansprucht werden sollen: 100 çg/g ergðben bei einer angenommenen tðglichen Hausstaub-Aufnahme von 100 mg durch Kleinkinder eine DEHP-Zufuhr von 10 çg/d, die einer resorbierten DEHP-Aufnahme von 5 çg/d entsprðchen. Bei einer unterstellten relevanten Exposition an 300 Tagen im Jahr ergðbe das ■bers Jahr eine resorbierte DEHP-Aufnahme von 4,1 çg/d. Dieser Tagesdosis entspricht bei einem Kleinkind mit 10 kg K—rpergewicht eine K—rperdosis von 0,41 çg/kg KG/d. Das wðren ca. 10% des TDI-Wertes von 4 çg/kg KG/d. Ein Richtwert f■r Kleinkinder f■r DEHP im Hausstaub in gleicher H—he ist bereits von der Arbeitsgemeinschaft —kologischer Forschungsinstitute e.V. (AGøF) aufgestellt worden, wenn auch ohne toxikologische Begr■ndung (AGøF 2004).
AGøF (2004) AGøF-Orientierungswerte f■r Inhaltsstoffe von Raumluft und Hausstaub. Umwelt & Gesundheit 1/2004:6-13
Akingbemi BT, Youker RT, Sottas CM, Ge R, Katz E, Klinefelter GR, Zirkin BR, Hardy MP (2001) Modulation of rat Leydig cell steroidogenic function by Di(2-ethylhexyl)phthalate. Biology of reproduction 65:1252-1259
Akingbemi BT, Ge R, Klinefelter GR, Zirkin BR, Hardy MP (2004) Phthalate-induced Leydig cell hyperplasia is associated with multiple endocrine disturbances. Proceedings of the National Academy of Sciences 101(3):775-780
Angerer und Koch (2004) Phthalate (Phthalsðurediester). Webseite: www.arbeitsmedizin.uni-erlangen.de/Koch_Phthalate.htm, zuletzt besucht am 15.06.2004
Arcadi FA, Costa C, Imperatore C, Marchese A, Rapisarda A, Salemi M, Trimarchi GR, Costa G (1998) Oral toxicity of Bis(2-ethylhexyl)phthalate during pregnancy and suckling in the Long-Evans Rat. Food and Chemical Toxicology 36(11):963-970
ARGUK (2004) Untersuchung von 499 Stðuben auf Diethylhexylphthalat (DEHP) im Zeitraum 1999 - 2004. Anlassbezogene Probenahme, unver—ffentlichte Labordaten.
ATSDR (2002) Toxicological Profile for Di(2-ethylhexyl)phthalate. US Department of Health and Human Services, Public Health Service, Agency for Toxic Substances and Disease Registry.
Baars AJ, Theelen RMC, Janssen PJCM, Hesse JM, van Apeldoorn ME, Meijerink MCM, Verdam L, Zeilmaker MJ (2001) Re-evaluation of human toxicological Maximum Permissible Risk levels. Rijksinstituut voor Volksgezondheid en Milieu (RIVM), Bilthoven. RIVM report 711701025
BAUCH (1991) Weichmacher in Innenrðumen. Materialien zur Umweltberatung 12/91. Beratung und Analyse Verein f■r Umweltchemie e.V., Wilsnacker Str. 15, 1000 Berlin 21
Becker K, Kaus S, Krause C, Lepom P, Schulz C, Seiwert M, Seifert B (2002) Umwelt-Survey 1998 Band V. Hausstaub: Stoffgehalte im Hausstaub aus Haushalten der Bev—lkerung in Deutschland. WaBoLu-Hefte 1/02. Hrsg: Umweltbundesamt, Postfach 330022, 14191 Berlin
BfR (2003) Tðgliche Aufnahme von Diethylhexylphthalat (DEHP). Stellungnsahme des BfR vom 23. Juli 2003. www.bfr.de/...
BGBl (2003) Kunststoffverordnung, Bundesgesetzblatt 2003/476, Teil A, Anlage 1
Bornehag CG, Sundell J, Weschler C, Sigsgaard T, Lundgren B, Hasselgren M, Hðgerhed-Engman L (2004) The Association between Asthma and Allergic Symptoms in Children and Phthalates in House Dust: A Nested Case-Control Study. Environmental Health Perspectives 112(14): 1393-1397
Butte W, Hoffmann W, Hostrup O, Schmidt A, Walker G (2001) Endokrin wirksame Substanzen im Hausstaub: Ergebnisse eines reprðsentativen Monitorings. Gefahrstoffe - Reinhaltung der Luft 61(1/2):19-23
Butte W (2004) Phthalate in Innenrðumen. Vortrag auf den 11. WaBoLu-Innenraumtagen, 17. - 19.5.2004. Institut f■r Wasser-, Boden- und Lufthygiene, Berlin
Calabrese EJ, Pastides H, Barnes R, Edwards C, Kostecki PT, Stanek III EJ, Veneman P, Gilbert CE (1989) How much soil do young children ingest: an epidemiological study. Regulatory Toxicology and Pharmacology 10:129-137
CPSC (2001) Report to the U.S. Consumer Product Safety Commission by the Chronic Hazard Advisory Panel on Diisononyl Phthalate (DINP), June 2001. U.S. Consumer Product Safety Commission, Directorate for Helath Sciences, Bethesda, MD 20814.
CSTEE (2002) Opinion on the results of the Risk Assessment of: Bis(2-ethylhexyl)phthalate (DEHP) Opinion expressed at the 29th plenary meeting, Brussels, 09 January 2002
CSTEE (2004) Opinion on the results of a second Risk Assessment of: Bis(2-ethylhexyl)phthalate [DEHP] Human Health Part, 41th plenary meeting of 8 January 2004
DFG (2003) MAK- und BAT-Werte-Liste 2003. Maximale Arbeitsplatzkonzentrationen und Biologische Arbeitsstofftoleranzwerte. Senatskommission zur Pr■fung gesundheitsschðdlicher Arbeitsstoffe, Mitteilung 39. Deutsche Forschungsgemeinschaft, Bonn.
Doull J, Cattley R, Elcombe C, Lake BG, Swenberg J, Wilkonson C (1999) in Koch et al. 2003
Duty MS, Singh NP, Silva MJ, Barr DB, Brock JW, Ryan L, Herrick RF, Christiani DC, Hauser R (2003a) The relationship between environmental exposures to phthalates and DNA damage in human sperm using the Neutral Comet Assay. Environmental Health Perspectives 111(9):1164-1169
Duty SM, Silva MJ, Barr DB, Brock JW, Ryan L, Chen Z, Herrick RF, Christiani DC, Hauser R (2003b) Phthalate exposure and human semen parameters. Epidemiology 14(3):269-277
ENDS (1999) Industry glimpses new challenges as endocrine science advances. Environmental Data Services (ENDS). Report 290:26-30
EU (1999) Entscheidung der Kommission der Europðischen Gemeinschaften vom 7. Dezember 1999 (1999/815/EG).
EU (2003a) Richtlinie 2003/15/EG, Kosmetikrichtlinie
EU (2003b) Directives 76/769 Anhang I, 67/548 Anhang I, 88/379. østerreichische Chemikalienverbotsverordnung 2003/477 Teil II.
Fromme H, Lahrz T, Piloty M, Gebhart H, Oddoy A, R■den H (2004) Occurrence of phathalates and musk fragrances in indoor air and dust from apartments and kindergartens in Berlin (Germany). Indoor Air 14(3):188
Gundert-Remy U (2004) Kinderspezifische Sicherheitsfaktoren bei der Ableitung von Grenzwerten. Umweltbedingte Gesundheitsrisiken Teil II. Hrsg.: Umweltbundesamt, Postfach 330022, 14191 Berlin. Download: www.umweltbundesamt.de
HH (2002) Schwerfl■chtige organische Umweltchemikalien in Hamburger
Hausstðuben. Hrsg.: Freie und Hansestadt Hamburg (HH), Umweltbericht 61/2002.
H—hr D, Abel J (1989) Zur Toxikologie des Phthalsðuredialkylesters DEHP. Umwelthygiene
22:93-109
IPCS (1992) Diethylhexyl Phthalate - Environmental Health Criteria 131. International Programme on Chemical Safety, World Health Organization, Genf. Download: www.inchem.org/documents/ehc/ehc/ehc131.htm
IRIS (2004) Integrated Risk Information System. Summary of Di(2-ethylhexyl)phthalate (DEHP); oral RfD assessment dated May 1991. US Environmental Protection Agency, Washington DC, USA.
Kahl R, Degen G, Foth H, Kramer P-J, Lilienblum W, Schrenk D, Schulz T, Schweinfurth (2003) Stellungnahme der Beratungskommission der Sektion Toxikologie der Deutschen Gesellschaft f■r experimentelle und klinische Pharmakologie und Toxikologie (DGPT) zu m—glichen Gesundheitsgefahren durch Di(2-ethylhexyl)phthalat (DEHP) aus Medizinprodukten in neonatalogischen Intensivstationen. Umweltmedizin in Forschung und Praxis 8(1):25-30
Koch HM, Drexler H, Angerer J (2003a) Die innere Belastung der Allgemeinbev—lkerung mit Di(2-ethylhexyl)phthalat (DEHP). Umweltmedizin in Forschung und Praxis 8(1):15-23
Koch HM, Drexler, H, Angerer J (2003b) An estimation of the daily intake of di(2-ethylhexyl)phthalate (DEHP) and other phthalates in the general population. International Journal of Hygiene and Environmental Health 206:77-83
Koch HM, Drexler H, Angerer J (2003c) Di(2-ethyl)hexylphthalat (DEHP)-Belastung von Kindergartenkindern im Vergleich zu Erwachsenen - Biologisches Monitoring spezifischer DEHP-Sekundðrmetabolite in Urin. Umweltmedizin in Forschung und Praxis 8(4):190Koch HM, Bolt HM, Angerer J (2004) Di(2-ethylhexyl)phthalate (DEHP) metabolites in human urine and serum after a single oral dose of deuterium-labelled DEHP. Archives of toxicology 78:123-130
Loff S, Kabs F, Witt K, Sartoris J, Mandl B, Niessen KH, Waag KL (2000) Polyvinylchloride infusion lines expose infants to large amounts of toxic plastizisers. J Pediatr Surg 35:1775-1781
MAFF, Department of Health and the Scottish Executive, Joint Food Safety and Standards Group (1996) Maff UK - Phthalates in food. Food surveillance information Sheet 82, March 1996
Meek ME, Chan PKL (1994) Bis(2-ethylhexyl)phthalate: evaluation of risks to health from environmental exposure in Canada. Journal of Environmental Science and Health Part C 12, 179-194
NTP-CERHR (2000) NTP-CERHR expert panel report on Di(2-ethylhexyl)phthalat. Federal Register 65(196), S. 60206 (erhðltlich auf der CERHR-Website: http://cerhr.niehs.nih.gov)
Persson PE, Penttinen H, Nuorteva P (1978) DEHP in the vicinity of an industrial area in Finland. Environmental Pollution 16:163-166
Petersen JH, Breindahl T (2000) Plasticizers in total diet samples, baby foos and infant formulae. Food Additives and Contaminants 17(2):133-141
P—hner A, Simrock S, Thumulla J, Weber S, Wirkner T (1997) Hintergrundbelastung des Hausstaubes von Privathaushalten mit mittel- und schwerfl■chtigen organischen Schadstoffen. Zeitschrift f■r Umweltmedizin 6:337-345
Poon R, Lecavalier P, Mueller R, Valli VE, Procter BG, Chu I (1997) Subchronic oral txicity of di-n-octyl phthalate and di(2-ehtylhexyl)phthalate in the rat. Food and Chemical Toxicology 35(2):225-239
Sheldon L, Whitaker D, Keever J, Clayton A, Perrit R (1993) Phthalates and PAHs in indoor and outdoor air in a Southern California community. Proceedings of Indoor Air Vol. 3
Straff W (2004) Was ist bei Kindern anders als bei Erwachsenen? Umweltbedingte Gesundheitsrisiken Teil I. Hrsg.: Umweltbundesamt, Postfach 330022, 14191 Berlin. Download: www.umweltbundesamt.de
Wolfe GW, Layton KA (2003) Multigeneration reproduction toxicity study in rats (unaudited draft): Diethylhexylphthalate: Multigenerational reproductive assessment by continuous breeding when administered to Sprague-Dawley rats in the diet. TherImmune Research Corporation (Gaithersburg, Maryland), TRC Study No 7244-200
WWF (2004) Faktenblðtter zu nachgewiesenen Chemikalien in der WWF
Blutprobenuntersuchung von Europaparlamentariern. www.wwf.de/imperia/md/content/pdf/umweltgifte/Blutuntersuchung
_Europaparlamentarier_-_Gifte.pdf, zuletzt besucht am 20.07.2004
Home | Inhalt
| Éber uns | Haftungsausschluss
| Gesundes Nest | Fertighaus
| Reiz- und Riechstoffe | Trinkwasser
Schadstoffbibliothek | Dienstleistungen | Pressemitteilungen | Diplomarbeiten | Kontakt